Câu 5: Cho 5,1 gam hỗn hợp Al và Mg tác dụng với lượng vừa đủ dung dịch H2SO4 9,8%, sau phản ứng thu được 5,6 lít khí H2 (ở đktc) a. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính nồng độ phần trăm của dung dịch X. Giúp mình với các b ơi

Những câu hỏi liên quan
Cho 5,1 gam hỗn hợp Al và Mg tác dụng với lượng vừa đủ dung dịch H2SO4 9,8%, sau phản ứng thu được 5,6 lít khí H2 (ở đktc)
(a) Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu.
(b) Tính nồng độ phần trăm của dung dịch X
a)\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: x 1,5x
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}27x+24y=5,1\\1,5x+y=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,1.27.100\%}{5,1}=52,94\%;\%m_{Mg}=100-52,94=47,06\%\)
b)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,1 0,15 0,05
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,1 0,1 0,1
\(m_{ddH_2SO_4}=\dfrac{\left(0,1+0,15\right).98.100}{9,8}=250\left(g\right)\)
mdd sau pứ = 5,1+250-0,15.2 = 254,8(g)
\(C\%_{ddAl_2\left(SO_4\right)_3}=\dfrac{0,05.342.100\%}{254,8}=6,71\%\)
\(C\%_{ddMgSO_4}=\dfrac{0,1.120.100\%}{254,8}=4,71\%\)
Đúng 3
Bình luận (0)
Hòa tan 5,1 gam Mg và Al vào dung dịch HCl 3,65%, sau phản ứng thu được 5,6 lít khí H2 (ở đktc) và dung dịch X. a) Tính phần trăm khối lượng của mỗi kim loại trong hỗn hợp đầu. b) Tính khối lượng mối khan có trong X c) Tính khối lượng dung dịch HCl đã dùng và nồng độ phần trăm của các chất trong X.
\(a)n_{Mg} = a ; n_{Al} = b \Rightarrow 24a +27b = 5,1(1)\\ Mg + 2HCl \to MgCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ n_{H_2} = a + 1,5b = \dfrac{5,6}{22,4} = 0,25(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,1\\ \%m_{Mg} = \dfrac{0,1.24}{5,1}.100\% = 44,44\%\ ;\ \%m_{Al} = 100\% -44,44\% = 55,56\%\\ b) n_{MgCl_2} = n_{Mg} = 0,1 \Rightarrow m_{MgCl_2} = 0,1.95 = 9,5(gam)\\ n_{AlCl_3} = n_{Al} = 0,1 \Rightarrow m_{AlCl_3} = 0,1.133,5 = 13,35(gam)\\ c)n_{HCl} = 2n_{Mg} + 3n_{Al} = 0,5(mol) \Rightarrow m_{dd\ HCl} = \dfrac{0,5.36,5}{3,65\%} = 500(gam)\)
\(m_{dd\ sau\ pư} = 5,1 + 500 - 0,25.2 = 504,6(gam)\\ C\%_{MgCl_2} = \dfrac{9,5}{504,6}.100\% = 1,89\%\\ C\%_{AlCl_3} = \dfrac{13,35}{504,6}.100\% = 2,65\%\)
Đúng 3
Bình luận (0)
Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí ở đktc. Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là: A. 21,74% và 78,26% B. 78,26% và 21,74% C. 88, 04% và 11,96% D. 11,96% và 88, 04%
Đọc tiếp
Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí ở đktc. Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là:
A. 21,74% và 78,26%
B. 78,26% và 21,74%
C. 88, 04% và 11,96%
D. 11,96% và 88, 04%
Đáp án A
Cho Mg và Ag tác dụng với HCl chỉ có Mg phản ứng.
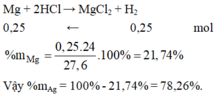
Đúng 0
Bình luận (0)
cho 2,16 gam hỗn hợp gồm Al và Cu tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng sau phản ứng thu được 0,672 lít khí ( đktc )
a) viết PTHH
b) tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu ?
c) tính nồng độ phần trăm của dung dịch H2SO4 đã dùng
a) PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b) \(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
_____0,02<---0,03<---------------------0,03
=> \(\left\{{}\begin{matrix}\%Al=\dfrac{0,02.27}{2,16}.100\%=25\%\\\%Cu=100\%-25\%=75\%\end{matrix}\right.\)
c) mH2SO4 = 0,03.98 = 2,94 (g)
=> \(C\%\left(H_2SO_4\right)=\dfrac{2,94}{200}.100\%=1,47\%\)
Đúng 1
Bình luận (0)
cho 9,7 gam hỗn hợp Zn và Cu tác dụng vừa đủ với 120 gam dung dịch HCl, sau phản ứng thu được dung dịch B, chất rắn C và 2,24 lít khí H2 ở ( đktc ). a. tính khối lượng mỗi kim loại trong hỗn hợp ban đầu? b. tính nồng độ phần trăm các chất trong dd B?
\(a)n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=n_{H_2}=n_{ZnCl_2}=0,1mol\\ m_{Zn}=0,1.65=6,5g\\ m_{Cu}=9,7-6,5=3,2g\\ b)C_{\%ZnCl_2}=\dfrac{0,1.136}{6,5+120-0,1.2}\cdot100=10,77\%\)
Đúng 3
Bình luận (0)
Câu 1: Cho 2,58 gam hỗn hợp Mg, Al tác dụng vừa đủ với V dung dịch H2SO4 0,5M loãng thu được 2,91362 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị VCâu 2: Cho 4,96 gam hỗn hợp Fe, Mg tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng a% thu được 3,136 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị aCâu 3: Cho 3,94 gam hỗn hợp Ba, Mg tác dụng vừa đủ với 100ml dung dịch H2SO4 xM loãng thu được 1,568 lít khí H2 (đktc). Tính khối lượng mỗi...
Đọc tiếp
Câu 1: Cho 2,58 gam hỗn hợp Mg, Al tác dụng vừa đủ với V dung dịch H2SO4 0,5M loãng thu được 2,91362 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị V
Câu 2: Cho 4,96 gam hỗn hợp Fe, Mg tác dụng vừa đủ với 200 gam dung dịch H2SO4 loãng a% thu được 3,136 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị a
Câu 3: Cho 3,94 gam hỗn hợp Ba, Mg tác dụng vừa đủ với 100ml dung dịch H2SO4 xM loãng thu được 1,568 lít khí H2 (đktc). Tính khối lượng mỗi kim loại trong hỗn hợp đầu và giá trị x
Câu 1:
\(n_{H_2}=\dfrac{2.91362}{22.4}=0.13mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2b 3b b 3b
Ta có: \(\left\{{}\begin{matrix}24a+54b=2.58\\a+3b=0.13\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0.04\\b=0.03\end{matrix}\right.\)
\(m_{Mg}=0.04\times24=0.96g\)
\(m_{Al}=0.03\times2\times27=1.62g\)
\(V_{H_2SO_4}=\dfrac{0.04+3\times0.03}{0.5}=0.26l\)
Câu 2:
\(n_{H_2}=\dfrac{3.136}{22.4}=0.14mol\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
a a a a
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}24a+56b=4.96\\a+b=0.14\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.09\\b=0.05\end{matrix}\right.\)
\(m_{Mg}=0.09\times24=2.16g\)
\(m_{Fe}=0.05\times56=2.8g\)
\(C\%_{H_2SO_4}=\dfrac{0.14\times98\times100}{200}=6.86\%\)
Đúng 0
Bình luận (0)
Câu 3:
\(n_{H_2}=\dfrac{1.568}{22.4}=0.07mol\)
\(Ba+H_2SO_4\rightarrow BaSO_4+H_2\)
a a a a
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b b b b
Ta có: \(\left\{{}\begin{matrix}137a+24b=3.94\\a+b=0.07\end{matrix}\right.\)\(\Leftrightarrow\left\{{}\begin{matrix}a=0.02\\b=0.05\end{matrix}\right.\)
\(m_{Ba}=0.02\times137=2.74g\)
\(m_{Mg}=0.05\times24=1.2g\)
\(CM_{H_2SO_4}=\dfrac{0.07}{0.1}=0.7M\)
Đúng 0
Bình luận (0)
Câu 1: Cho 11,9 gam hỗn hợp Zn và Al phản ứng vừa đủ với 125 gam dung dịch HCl. Sau phản ứng thu được 8,96 lít khí ở đktc a. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính nồng độ phần trăm của dung dịch HCl đã dùng
a)
Gọi $n_{Zn} = a(mol) ; n_{Al} = b(mol) \Rightarrow 65a + 27b = 11,9(1)$
$Zn + 2HCl \to ZnCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
Theo PTHH :
$n_{H_2} = a + 1,5b = \dfrac{8,96}{22,4} = 0,4(2)$
Từ (1)(2) suy ra : a = 0,1; b = 0,2
$m_{Zn} = 0,1.65 = 6,5(gam)$
$m_{Al} = 0,2.27 = 5,4(gam)$
b) $n_{HCl} = 2n_{H_2} = 0,8(mol)$
$C\%_{HCl} = \dfrac{0,8.36,5}{125}.100\% = 23,36\%$
Đúng 4
Bình luận (0)
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch HCl 10%, thu được 2,24 lít khí H 2 (ở đktc).
a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b/ Tính nồng độ % các muối có trong dung dịch sau phản ứng.
cho 3,79 (G) hỗn hợp Zn và Al tác dụng với dung dịch H2SO4 loãng dư .Sau phản ứng thu được 1,792 lít khí (đktc)
a)tính khối lượng mỗi kim loại
b) tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu
PTHH:
Zn + H2SO4 ---> ZnSO4 + H2 (1)
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
Ta có: \(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
Gọi x, y lần lượt là số mol của Zn và Al
a. Theo PT(1): \(n_{H_2}=n_{Zn}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}y\left(mol\right)\)
=> \(x+\dfrac{3}{2}y=0,8\) (*)
Theo đề, ta có: 65x + 27y = 3,79 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+\dfrac{3}{2}y=0,8\\65x+27y=3,79\end{matrix}\right.\)
(Ra số âm, bn xem lại đề nhé.)
Đúng 0
Bình luận (0)






















